Дмпп сердца легочная артерия. Причины появления дефекта межпредсердной перегородки сердца и лечение патологии
На здоровье будущего малыша влияет много факторов. Неправильное внутриутробное развитие может вызвать врожденный порок внутренних органов. Одним из расстройств является дефект межжелудочковой перегородки сердца (дмжп), который встречается в трети случаев.
Особенности
Дмжп является к врожденным порокам сердца (впс). В результате патологии образуется отверстие, соединяющее нижние камеры сердца: его желудочки. Уровень давления в них разный, из-за чего при сокращениях сердечной мышцы немного крови из более мощной левой части попадает в правую. В результате ее стенка растягивается и увеличивается, нарушается кровоток малого круга, за который отвечает правый желудочек. Из-за повышения давления венозные сосуды перегружаются, возникают спазмы, уплотнения.
Левый желудочек отвечает за кровоток в большом круге, поэтому он мощнее и имеет более высокое давление. При патологическом протекании артериальной крови в правый желудочек необходимый уровень давления снижается. Для поддержания нормальных показателей желудочек начинает работать с большей силой, что еще прибавляет нагрузку на правую часть сердца и приводит к его увеличению.
Количество крови в малом круге возрастает и правому желудочку приходится повышать давление, чтобы обеспечить нормальную скорость прохождения по сосудам. Так возникает обратный процесс – давление в малом круге теперь становится выше и кровь из правого желудочка протекает в левый. Обогащенная кислородом кровь разбавляется венозной (обедненной), в органах и тканях возникает недостаток кислорода.
Такое состояние наблюдается при больших отверстиях и сопровождается нарушением дыхания и сердечного ритма. Зачастую диагноз ставится в первые несколько дней жизни малыша, и врачи начинают незамедлительное лечение, готовят к операции, при возможности избежать операции проводят регулярное наблюдение.
Дмжп маленьких размеров может сразу не проявиться, или не диагностируется по причине слабо выраженной симптоматики. Поэтому важно знать о возможных признаках наличия этого вида впс, чтобы своевременно принять меры и провести лечение ребенка.
Кровоток у новорожденных

Сообщение между желудочками не всегда является патологическим отклонением. У плода при внутриутробном развитии легкие не участвуют в обогащении крови кислородом, поэтому в сердце есть открытое овальное окно (ооо), через него выполняется перетекание крови из правой части сердца в левую.
У новорожденных легкие начинают работать и ооо постепенно зарастает. Полностью окно закрывается в возрасте около 3 месяцев, у некоторых не считается патологией зарастание к 2 годам. При некоторых отклонениях ооо может наблюдаться у детей в 5 – 6 лет и старше.
В норме у новорожденных ооо не больше 5 мм, при отсутствии признаков сердечно-сосудистых заболеваний и других патологий это не должно вызывать опасений. Доктор Комаровский рекомендует постоянно следить за состоянием малыша, регулярно посещать детского кардиолога.
Если же размер отверстия 6 -10 мм, это может быть признаком дмжп, требуется хирургическое лечение.
Виды дефекта

Сердечная перегородка может содержать одно или несколько патологических отверстий разного диаметра (например, 2 и 6 мм) – чем их больше, тем сложнее степень заболевания. Размер их варьируется от 0,5 до 30 мм. При этом:
- Дефект размером до 10 мм – считается малым;
- Отверстия от 10 до 20 мм – средние;
- Дефект свыше 20 мм является крупным.
По анатомическому разделению дмжп у новорожденного бывает трех типов и различается по месту локализации:
- В перепончатой (верхней части сердечной перегородки) отверстие возникает в больше чем 80% случаев. Дефекты в форме круга или овала достигают 3см, если они небольшие (около 2 мм), то способны самопроизвольно закрываться в процессе взросления ребенка. В некоторых случаях зарастают дефекты 6 мм, нужна ли операция, решает врач, ориентируясь на общее состояние ребенка, особенности протекания болезни.
- Мышечный джмп в средней части перегородки встречается реже (около 20 %), в большинстве случаев круглой формы, при размере 2 – 3 мм могут закрыться с возрастом ребенка.
- На границе выводящих сосудов желудочков образуется надгребневый дефект перегородки – самый редкий (примерно 2 %), и почти не купируется самостоятельно.
В редких случаях встречается сочетание нескольких видов джмп. Дефект может быть самостоятельной болезнью, или сопутствовать другим тяжелым отклонениям в развитии сердца: дефекту межпредсердной перегородки (дмпп), проблемам с артериальным кровотоком, коарктации аорты, стенозам аорты и легочной артерии.
Причины развития

Дефект формируется у плода с 3 недель до 2,5 месяцев внутриутробного развития. При неблагоприятном течении беременности могут возникать патологии в строении внутренних органов. Факторы, увеличивающие риск возникновения дмжп:
- Наследственность. Предрасположенность к дмжп может передаваться генетически. Если у кого из близких родственников наблюдались пороки различных органов, в том числе и сердца, велика вероятность возникновения отклонений у ребенка;
- Вирусные заболевания инфекционного характера (грипп, краснуха), которые женщина перенесла в первые 2,5 месяца беременности. Опасность представляют также герпес, корь;
- Прием лекарственных средств – многие из них могут вызывать интоксикацию эмбриона и приводить к образованию различных пороков. Особенно опасными являются антибактериальные, гормональные, лекарства против эпилепсии и воздействующие на цнс;
- Вредные привычки у матери – алкоголь, табакокурение. Этот фактор, особенно в начале беременности, увеличивает риск возникновения отклонений у плода в несколько раз;
- Наличие хронических заболеваний у беременной женщины – сахарный диабет, проблемы нервной, сердечной системы и подобные могут провоцировать патологии у малыша;
- Авитаминоз, дефицит необходимых питательных веществ и микроэлементов, строгие диеты во время беременности увеличивают риск возникновения врожденных пороков;
- Тяжелые токсикозы на ранних сроках беременности;
- Внешние факторы – опасная экологическая обстановка, вредные условия труда, повышенная утомляемость, перенапряжение и стрессы.
Наличие этих факторов не всегда вызывает возникновение тяжелых заболеваний, но увеличивает эту вероятность. Чтобы снизить ее, нужно по возможности ограничить их воздействие. Вовремя принятые меры по предотвращению проблем в развитии плода являются хорошей профилактикой врожденных заболеваний у будущего ребенка.
Возможные осложнения

Дефекты маленького размера (до 2 мм) при нормальном состоянии малыша не являются угрозой для его жизни. Необходим регулярный осмотр, наблюдение у специалиста и способны со временем самопроизвольно купироваться.
Отверстия большого размера вызывают нарушение работы сердца, которое проявляется в первые дни жизни малыша. Дети с дмжп тяжело переносят простудные и инфекционные заболевания, зачастую с осложнениями на легкие, пневмонией. Они могут развиваться хуже сверстников, тяжело переносят физические нагрузки. С возрастом одышка возникает даже в состоянии покоя, появляются проблемы с внутренними органами из-за кислородного голодания.
Межжелудочковый дефект может вызывать серьезные осложнения:
- Легочную гипертензию – повышение сопротивления в сосудах легких, которое вызывает правожелудочковую недостаточность и развитие синдрома Эйзенменгера;
- Нарушение работы сердца в острой форме;
- Воспаление внутренней сердечной оболочки инфекционного характера (эндокардит);
- Тромбозы, угрозу инсульта;
- Сбои в работе сердечных клапанов, формирование клапанных сердечных пороков.
Чтобы минимизировать пагубные для здоровья малыша последствия, необходима своевременная квалифицированная помощь.
Симптомы

Клинические проявления заболевания обусловлены размерами и местонахождением патологических отверстий. Небольшие дефекты перепончатой части сердечной перегородки (до 5 мм) протекают в некоторых случаях без симптоматики, иногда первые признаки возникают у детей от 1 до 2 лет.
В первые дни после рождения у младенца можно услышать сердечные шумы, вызванные перетеканием крови между желудочками. Иногда можно ощутить небольшую вибрацию, если положить руку на грудь малыша. В последствии шум может ослабевать, когда ребенок в вертикальном положении или испытал физические нагрузки. Это вызвано сжатием мышечной ткани в области отверстия.
Крупные дефекты могут обнаружиться у плода еще до или в первое время после рождения. Из-за особенностей кровотока при внутриутробном развитии у новорожденных нормальный вес. После рождения система перестраивается на обычную и отклонение начинает проявлять себя.
Особенно опасны маленькие дефекты, находящиеся в нижней области сердечной перегородки. Они могут не проявлять симптомов в первые несколько дней жизни ребенка, но в течение некоторого времени формируется нарушение дыхание и работы сердца. При внимательном отношении к ребенку можно вовремя заметить симптомы заболевания и обратиться к специалисту.
Признаки возможной патологии, о которых необходимо сообщить педиатру:
- Бледность кожных покровов, посинение губ, кожи вокруг носа, ручек, ножек при нагрузке (плаче, криках, перенапряжении);
- Младенец теряет аппетит, устает, часто бросает грудь во время кормления, медленно набирает вес;
- Во время физических нагрузок, плача у малышей появляется одышка;
- Повышенное потоотделение;
- Грудничок старше 2 месяцев вялый, сонливый, у него снижена двигательная активность, наблюдается задержка в развитии;
- Частые простуды, которые тяжело лечатся и перетекают в пневмонию.
При выявлении подобных признаков проводится обследование грудничка для выявления причин.
Диагностика

Проверить состояние и работу сердца, выявить заболевание позволяют следующие методы исследования:
- Электрокардиограмма (ЭКГ). Позволяет определить перегруженность сердечных желудочков, выявить наличие и степень гипертензии легких;
- Фонокардиография (ФКГ). В результате исследования возможно выявление шумов сердца;
- Эхокардиография (ЭхоКГ). Способно выявлять нарушения кровотока и помогает подозревать дмжп;
- Ультразвуковое исследование. Помогает оценить работу миокарда, уровень давления артерии легкого, количество сбрасываемой крови;
- Рентгенография. По снимкам грудной клетки возможно определение изменений легочного рисунка, увеличение размеров сердца;
- Зондирование сердца. Позволяет определить уровень давления в артерии легких и желудочке сердца, повышенное содержание кислорода в венозной крови;
- Пульсоксиметрия. Помогает выяснить уровень содержания кислорода в крови – недостаток говорит о нарушениях в сердечно-сосудистой системе;
- Катетеризация сердца. Помогает оценить состояние структуры сердца, выяснить уровень давления в сердечных желудочках.
Лечение

Дмжп 4 мм, иногда до 6 мм – маленького размера – при отсутствии нарушения дыхательного, сердечного ритма и нормальном развитии ребенка позволяет в некоторых случаях не использовать хирургическое лечение.
При ухудшении общей клинической картины, появлении осложнений возможно назначение операции в 2 – 3 года.
Хирургическое вмешательство проводится с подключением пациента к аппарату искусственного кровообращения. Если дефект меньше 5 мм, его стягивают швами в форме П. При размерах отверстия больше 5 мм, его прикрывают с помощью заплаток из искусственного или специально подготовленного био-материала, зарастающего в последствии собственными клетками организма.
Если необходимо оперативное лечение ребенку в первые недели жизни, но оно невозможно по некоторым показателям здоровья и состояния малыша, ему накладывают временную манжетку на легочную артерию. Она помогает выравнивать давление в желудочках сердца и облегчает состояние пациента. Спустя несколько месяцев манжету удаляют и проводят операцию по закрытию дефектов.
Определение
Дефект межпредсердной перегородки-врожденный порок сердца, при котором есть сообщение между двумя предсердиями, развивающееся в результате аномального развития первичной и вторичной межпредсердных перегородок и эндокардиальных подушек.
Дефект межпредсердной перегородки в сочетании со стенозом левого атриовентрикулярного отверстия носит название синдрома Лютамбаше.
Эпидемиология
Распространенность дефекта межпредсердной перегородки составляет 5-10% всех врожденных пороков, является наиболее частым пороком сердца у взрослых (30%), у женщин отмечают чаще, чем у мужчин (2:1).
Патологическая анатомия
Существует несколько морфологических типов дефекта межпредсердной перегородки. Наиболее частый вариант - высокий дефект межпредсердной перегородки типа ostium secundum (75% случаев), возникающий вследствие нарушения развития вторичной перегородки, локализуется в центральной части межпредсердной перегородки в области овальной ямки (рис. 3.3).
Дефект типа ostium primum (15%) представляет собой вариант дефекта эндокарда, возникает вследствие неполного развития первичной перегородки, располагается в нижнем отделе перегородки непосредственно над уровнем предсердно-желудочковых отверстий, сочетается с расщеплением створок митрального и реже трехстворчатого клапанов.
Сочетание нарушения развития перегородок предсердия с неправильным расположением венозного синуса приводит к образованию сложных дефектов.
Дефекты венозного синуса (10%) чаще отмечают высоко в межпредсердной перегородке вблизи от впадения верхней полой вены, связаны с атипичным впадением легочных вен в правое предсердие или верхнюю полую вену. Намного реже дефекты венозного синуса могут локализоваться в нижней части перегородки над устьем нижней полой вены.
В некоторых случаях отмечают общее предсердие - отсутствие большей части межпредсердной перегородки или наличие только рудиментарных ее элементов, часто сочетается с расщеплением атриовентрикулярных клапанов.
Открытое овальное отверстие, которое не закрывается у 20% взрослых, не следует рассматривать как разновидность дефекта межпредсердной перегородки, поскольку при истинном дефекте имеется недостаточность ткани, а при открытом овальном окне сообщение осуществляется за счет клапана, который открывается при особых обстоятельствах.
Синдром Лютамбаше морфологически характеризуется наличием дефекта межпредсердной перегородки (чаще вторичного) и сужения левого атриовентрикулярного отверстия (врожденного или приобретенного). Характерным является расширение ЛА, которая иногда вдвое превышает размер аорты.
Нарушения гемодинамики
Наличие дефекта межпредсердной перегородки приводит к сбросу артериальной крови из левого предсердия в правое вследствие наличия градиента давления между ними. В результате возникает перегрузка объемом правой половины сердца, дилатация ПЖ и увеличение ОЦК в малом круге. При больших дефектах это может приводить к легочной гипертензии, однако выраженная гипертензия в малом круге в первые 20 лет возникает у около 2% больных.
Основную роль в компенсации нарушения кровообращения играет ПЖ, работа которого увеличивается в несколько раз. Недостаточность ПЖ развивается после 10 лет существования порока, в более старшем возрасте присоединяется недостаточность ЛЖ. Последняя, вызывая уменьшение его податливости, может приводить к увеличению объема шунта слева направо.
При синдроме Лютамбаше величина шунта увеличивается пропорционально возрастанию стенозирующего дефекта митрального отверстия, помимо этого происходит нарушение оттока крови из малого круга и возникновение легочной гипертензии.
Клиническая картина
Клинические проявления порока зависят от степени нарушения гемодинамики и изменяются с возрастом. При относительно небольшом дефекте в молодом возрасте больные могут не предъявлять жалоб и порок выявляют при случайном обследовании. Жалобы на одышку и приступы сердцебиений при физической нагрузке возникают в возрасте старше 40 лет, затем нарастают слабость и утомляемость, появляются различные аритмии, СН, которая обусловлена выраженной легочной гипертензией.
При больших дефектах межпредсердной перегородки одышка является одним из симптомов заболевания уже в молодом возрасте. У больных часто возникают приступы сердцебиения.
При перкуссии отмечают расширение границ сердца преимущественно вправо, а при больших дефектах - влево. В отдельных случаях описаны наличие сердечного горба (за счет увеличения правых отделов сердца), а также систолическое дрожание у левого края грудины.
Характерна аускультативная картина: над ЛА слева у грудины выслушивается систолический шум умеренной интенсивности, возникающий вследствие увеличенного кровотока через клапан ЛА. Второй тон над ЛА усилен и раздвоен. Реже определяют диастолический шум над нижней частью грудины, связанный с относительным стенозом отверстия трехстворчатого клапана при увеличенном количестве крови, проходящей через него. После того как возросшее легочное сосудистое сопротивление приводит к понижению величины сброса крови слева направо, интенсивность шумов снижается, появляется диастолический шум, вызванный недостаточностью клапана ЛА.
Диагностика
На ЭКГ электрическая ось сердца у больных со вторичным дефектом отклонена вправо, с первичным - влево. При каждом из дефектов выявляют различную степень перегрузки и гипертрофии ПЖ и правого предсердия, выраженность которой зависит от величины давления в легочном стволе. Выявляют признаки частичной блокады правой ножки пучка Гиса (феномен rSR"или rsR" в правых грудных отведениях), могут определять предсердную экстрасистолическую аритмию, пароксизмальную суправентрикулярную тахикардию. У больных с синдромом Лютамбаше нередко выявляют фибрилляцию предсердий.
На рентгенограмме сердце увеличено в поперечнике, в косых проекциях определяется увеличение правых отделов сердца. Дуга ЛА выбухает, дуга аорты уменьшена, усилен сосудистый рисунок легких, корни легких расширены, характерна их пульсация.
Диагноз устанавливают методом трансторакальной и допплеровской эхо КГ, с помощью которой можно установить локализацию, размер дефекта (хорошо визуализируются оstium secundum и primum), а также направление сброса крови. При эхоКГ-исследовании выявляют следующие признаки:
Увеличение полости правого предсердия и ПЖ;
Парадоксальное движение межжелудочковой перегородки;
Гипердинамичное движение стенок левого предсердия;
Признаки легочной гипертензии;
Признаки расщепления митрального и трехстворчатого клапанов с проявлениями их недостаточности при первичном дефекте (рис. 3.4);

Пролапс митрального клапана при вторичном дефекте;
Стеноз митрального отверстия при синдроме Лютамбаше;
Шунтирование крови между предсердиями слева направо или справа налево (рис. 3.5а, б).
Дефекты венозного синуса требуют дополнительных диагностических подходов - чреспищеводная эхоКГ обеспечивает наилучшую визуализацию межпредсердной перегородки, легочных вен, особенно у взрослых пациентов с недостаточными «акустическими окнами».

В-режим: а) субкостальная позиция, длинная ось; б) апикальная четырехкамерная позиция, шунт слева направо (левое предсердие - правое предсердие)
Катетеризации полостей сердца обычно не требуется, кроме случаев сопутствующей легочной гипертензии или когда неинвазивное исследование неполноценно. Наличие дефекта межпредсердной перегородки подтверждается проведением катетера из правого предсердия через перегородку в левое и повышением насыщения крови кислородом в полости правого предсердия по сравнению с пробами крови, взятой у устья полых вен. Разница в 2 об.% и более (или 8-10%) рассматривается как абсолютный признак шунтирования крови.
Коронароангиографию обычно проводят пациентам в возрасте старше 40 лет перед планируемой хирургической коррекцией порока.
Дефект межпредсердной перегородки также может быть диагностирован с помощью КТ (рис. 3.6) или МРТ, которая является методом выбора для оценки внесердечной анатомии, в том числе больших сосудов, ветвей ЛА, также как и системных и легочных венозных соединений.

Рис. 3.6.
Мультиспиральная КТ, апикальный срез
Хирургическое закрытие дефекта рекомендовано, если соотношение легочного к системному кровотоку более чем 1,5:1 и отношение легочного к системному сосудистому сопротивлению менее 0,7. Нет единого мнения относительно хирургического лечения асимптомных больных в возрасте 25-40 лет, однако оно оправдано для предупреждения прогрессирования симптомов. Вследствие возможности увеличения сброса крови слева направо, появления фибрилляции предсердий и развития легочной гипертензии с возрастом желательно выполнение хирургической коррекции порока до появления признаков ухудшения функции сердца. У симптомных больных в возрасте старше 40 лет хирургическое закрытие дефекта улучшает толерантность к физической нагрузке и выживаемость по сравнению с медикаментозной терапией и предотвращает дальнейшее ухудшение функционального состояния, хотя не снижает риск развития суправентрикулярной аритмии, СН и цереброваскулярных событий. Хирургическое вмешательство у 80% больных старше 60 лет со значительным сбросом крови приводит к улучшению симптомов. У 70% больных старшего возраста после операции сохраняются нарушения ритма, у 10-25% они возникают впервые, повышается риск системной АГ неясной этиологии.
Показания к хирургическому лечению
Неэффективная медикаментозная терапия СН;
Значительный артериовенозный сброс;
Отставание в физическом развитии;
Повышение давления в малом круге кровообращения.
Противопоказания к оперативному вмешательству
1. Веноартериальный (справа налево) сброс, поскольку это признак выраженной гипертензии и часто необратимых изменений в малом круге кровообращения.
2. Выраженная левожелудочковая недостаточность.
Хирургическое лечение заключается в ушивании или пластике заплатой дефекта межпредсердной перегородки. Мелкие дефекты зашивают, большие закрывают гомотрансплантатами или протезами из пластмассовой губки. При первичном дефекте со значительной митральной недостаточностью дополнительно ушивают расщепленную створку или проводят протезирование митрального клапана. В результате хирургического лечения улучшается состояние больного: уменьшаются одышка, сердцебиение, размеры сердца.
В последние годы возрастает роль устройств для закрытия дефекта (впервые применены в 1976 г.), выбор типа устройства зависит от локализации дефекта. В настоящий момент нет сравнительных исследований между внедрением устройств и хирургическими методами операции, не существует консенсуса по длительному наблюдению после установки устройств и долговременные исходы неизвестны, включая риск развития предсердной аритмии, СН и инсульта, предполагается, что исход будет сопоставим.
При синдроме Лютамбаше хирургическое лечение заключается в одномоментной коррекции - устранении дефекта межпредсердной перегородки и митральной комиссуротомии. Противопоказаниями к операции служат лишь тяжелая стадия легочной гипертензии и резко выраженная дистрофия миокарда, обусловливающая терминальную стадию СН.
Медикаментозная терапия включает симптоматические средства: антиаритмические препараты при фибрилляции предсердий и пароксизмальной суправентрикулярной тахикардии, лечение СН.
Вторичный дефект имеет благоприятное естественное течение в первые 20-30 лет жизни. Причиной смерти при отсутствии оперативной коррекции является правожелудочковая СН, реже - тромбоз ЛА, аритмия. При первичном дефекте течение менее благоприятное, прогноз хуже, раньше возникают клиническая симптоматика и осложнения, основным отягощающим фактором является легочная гипертензия.
– дефект межпредсердной перегородки , один из часто встречающихся пороков сердца . У этого порока есть частный подвид, который называют Открытое Овальное Окно (ООО) . Само по себе Открытое Овальное Окно не является пороком сердца , так как внутри этого окна есть специальный клапан, который закрывает его и не даёт крови перетекать из левого предсердия в правое. Однако если этот клапан окажется неисправным, то такая ситуация называется ООО со сбросом слева направо и уже является пороком сердца . Однако, что делать если у ребёнка обнаружили – надо ли его закрывать? Нужна ли операция при ДМПП? С этими вопросами мы постараемся разобраться в этой статье.
Сам по себе бывает разных вариантов и разных расположений. Он может располагаться как мышечной части перегородки , так и в мембранной , а может располагаться с краю перегородки, тогда говорят что дефект не имеет одного края . Также встречается ещё и решётчатый ДМПП который представляет из себя множество мелких дефектов межпредсердной перегородки .
Авторские права на представленный материал принадлежат сайтуКроме этого, может быть как самостоятельным пороком сердца, так и являться частью сложных пороков сердца , таких как АВК (атрио-вентикулярный канал) , Тетрада Фалло , гипоплазия желудочка и тд. В этой статье мы коснёмся только тех случаев когда является единственным и самостоятельным пороком сердца .
Давайте посмотрим на систему кровообращения ребёнка , который ещё не родился. Как известно, у человека имеется два круга кровообращения : большой, который доставляет кровь к органам и тканям и малый, который доставляет кровь от сердца к лёгким. При этом большой круг кровообращения проходит через правое предсердие , а малый круг кровообращения – через левое. Однако у будущего ребёнка, который ещё не родился, лёгкие не функционируют, поэтому малый круг кровообращения ему не нужен. То есть у неродившегося ребёнка наличие ДМПП не мешает ему нормально развиваться в утробе матери! То есть до родов о состоянии ребёнка можно не беспокоиться.
Теперь посмотрим что происходит после родов. Как только ребёнок сделает первый вздох, у него начинает функционировать малый круг кровообращения . При этом уменьшается давление в легочной артерии, клапан в ООО закрывается, а само ООО потом зарастает. Однако, если в предсердиях между малым и большим кругом имеется сообщение в виде , то тут можно рассматривать две ситуации:
- Очень большой ДМПП – в этом случае, так как давление в правом предсердии меньше чем давление в левом, то происходит сброс слева-направо. То есть кровь которая приходит из лёгких попадает из левого предсердия в правое, затем в правый желудочек и снова в лёгкие. В этом случае правые отделы сердца переполняются кровью и легочной круг не может нормально функционировать. В большом, основном круге кровообращения происходит обратный процесс – ему крови не хватает. В результате ребёнок не может нормально развиваться и ему требуется срочная операция. Радует то, что подобные пороки сердца встречаются очень редко.
- Маленький ДМПП – маленькими считаются дефекты размерами менее 10 мм. Как правило в раннем возрасте такие дефекты не приводят к каким либо отрицательным последствиям – ребёнок развивается нормально, у него нет каких либо признаков сердечной недостаточности . В таком случае срочная операция не требуется, можно подождать пока ребёнок достигнет оптимального возраста в 3-5 лет, и безопасно закрыть дефект. В некоторых случая дефект закрывается сам, за счёт развития и расширения сердечной мышцы.
А что будет, если дефект межпредсердной перегородки не закрывать совсем? В таком случае, по мере взросления ребёнка и увеличения нагрузки на сердце, будет нарастать перегрузка правых отделов сердца. Правое предсердие будет увеличиваться в размерах, что негативно скажется на его сократительной способности, и на работе клапанов. Кроме того в стенке правого предсердия находятся специальные проводящие волокна , которые задают ритм сердца и обеспечивают его сокращения. При увеличении правого предсердия целостность этих волокон нарушается и могут возникать нарушения ритма сердца. Также при переполнении кровью легочной артерии, в лёгких возникает застой крови, что приводит к возникновению частых воспалительных заболеваний в лёгких, трудно поддающихся лечению. Таким образом вывод может быть только один: если показана операция, то её необходимо сделать в оптимальные сроки , иначе затягивание с операцией может привести к целому ряду негативных последствий.
Теперь поговорим о видах коррекции ДМПП, или другими словами, какие бывают операции? Существует два основных метода коррекции ДМПП :
- Открытая полосная операция – это традиционный метод, который широко использовался на заре кардиохирургии. При такой операции разрезаются рёбра в хрящевой части, вскрывается грудная клетка, организм пациента охлаждается, сердце останавливается, магистральные сосуды подключают к специальному прибору – оксигенатору, который обеспечивает искусственное кровообращение. Сердце разрезают, затем зашивают отверстия в перегородке (либо ставят заплату), затем сшивают сердечную мышцу, нагревают организм, запускают сердце, и отключают прибор искусственного кровообращения. Достоинства этого метода заключаются в том, что таким способом можно исправить практически все виды ДМЖП, а заодно хирург может скорректировать другие пороки сердца, если они имеются.
- Эндоваскулярная операция – суть этого метода заключается в том, что грудная клетка не вскрывается, и сердце не останавливается. Вместо этого делается небольшой прокол на ноге, через него в бедренную артерию вводят специальное устройство – , которое проталкивается в предсердие , и там с помощью этого окклюдера закрывается дефект. Достоинства этого заключаются метода в том, что такая операция менее травматичная, восстановление происходит в течении одного дня и меньше риск для пациента. Недостатком этого метода является его ограниченная применяемость. Этот метод сам по себе дорогой, требует наличия высокой квалификации от медперсонала, а также уникального оборудования. Кроме того, далеко не все виды могут быть закрыты таким способом.
Тем не менее во всем мире, закрытие дефекта межпредсердной перегородки окклюдером является предпочтительным методом. В наше стране ещё можно встретить кардиологов и кардиохирургов, которые либо ничего не знают об эндоваскулярных методах закрытия ДМПП, либо начинают рассказывать много ужасов о возможных осложнениях после подобной операции. Особенно много таких кардиохирургов работает в Иркутском кардиодиспансере .
Дата публикации статьи: 15.05.2017
Дата обновления статьи: 21.12.2018
Из этой статьи вы узнаете: что такое дефект межпредсердной перегородки, почему он возникает, к каким осложнениям может привести. Как выявляют и лечат этот врожденный .
Дефект межпредсердной перегородки (сокращенно ДМПП) – это один из самых частых врожденных пороков сердца, при котором в перегородке, разделяющей правое и левое предсердие, существует отверстие. При этом пороке из левого предсердия кровь, обогащенная кислородом, попадает напрямую в правое предсердие.
В зависимости от размеров отверстия и существования других пороков, эта патология может или не иметь никаких негативных последствий, или приводить к перегрузке правых отделов сердца, и нарушениям сердечного ритма.
Открытое отверстие в межпредсердной перегородке присутствует у всех новорожденных детей, так как оно необходимо для кровообращения у плода во время внутриутробного развития. Сразу же после родов отверстие закрывается у 75% детей, однако у 25% взрослых оно остается открытым.
Пациенты с наличием данной патологии могут не иметь никаких симптомов в детском возрасте, хотя время их появления зависит от величины отверстия. Клиническая картина в большинстве случаев начинает проявляться с увеличением возраста. В возрасте 40 лет 90% людей с этим пороком, которым не проводилось лечение, страдают от одышки при физической нагрузке, усталости, сердцебиения, нарушений сердечного ритма и сердечной недостаточности.
Занимаются проблемой дефекта в межпредсердной перегородке педиатры, кардиологи и кардиохирурги.
Причины патологии
Межпредсердная перегородка (МПП) разделяет левое и правое предсердия. Во время внутриутробного развития в ней есть отверстие, называемое овальным окном, которое позволяет крови переходить из малого круга в большой, минуя легкие. Так как плод в это время получает все питательные вещества и кислород через плаценту от матери – малый круг кровообращения, основная задача которого состоит в обогащении крови кислородом в легких во время дыхания, ему не нужен. Сразу же после рождения, когда ребенок делает свой первый вдох и расправляет легкие, это отверстие закрывается. Однако так случается не у всех детей. У 25% взрослых наблюдается незакрытое овальное окно.
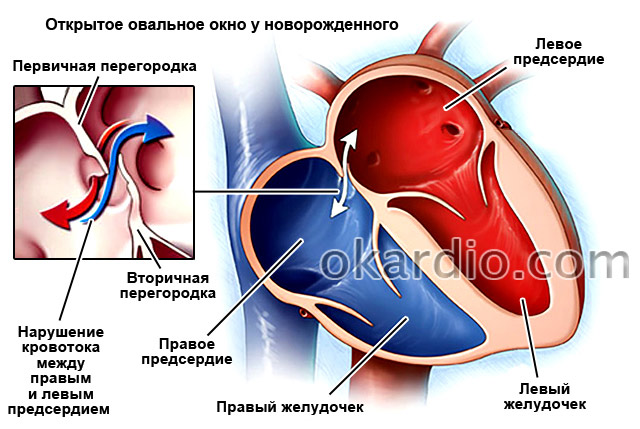
Дефект может появляться во время внутриутробного развития плода и в других частях МПП. У некоторых пациентов его возникновение может быть связано со следующими генетическими заболеваниями:
Однако у большинства пациентов причину появления ДМПП выяснить не удается.
Прогрессирование болезни
У здоровых людей уровень давления в левой половине сердца значительно выше, чем в правой, поскольку левый желудочек прокачивает кровь по всему организму, тогда как правый – лишь через легкие.
При наличии большого отверстия в МПП кровь из левого предсердия сбрасывается в правое – возникает так называемый шунт, или сброс крови слева направо. Этот дополнительный объем крови приводит к перегрузке правых отделов сердца. Без лечения это состояние может вызвать увеличение их размеров и привести к сердечной недостаточности.
Любой процесс, который повышает давление в левом желудочке, может усилить сброс крови слева направо. Это может быть артериальная гипертензия, при которой увеличивается артериальное давление, или ишемическая болезнь сердца, при которой повышается жесткость сердечной мышцы и снижается ее эластичность. Именно поэтому клиническая картина дефекта МПП развивается у людей старшего возраста, а у детей чаще всего эта патология протекает бессимптомно. Усиление шунта крови слева направо повышает давление в правых отделах сердца. Их постоянная перегрузка вызывает увеличение давления в легочной артерии, которое приводит к еще большей перегрузке правого желудочка.
Этот замкнутый круг, если его не разорвать, может привести к тому, что давление в правых отделах превысит давление в левой половине сердца. Это становится причиной возникновения сброса справа налево, при котором в большой круг кровообращения попадает венозная кровь, которая содержит небольшое количество кислорода. Появление шунта справа налево называют синдромом Эйзенменгера, это считается неблагоприятным прогностическим фактором.
Харктерные симптомы
Размер и расположение отверстия в МПП влияет на симптомы этого заболевания. Большинство детей с ДМПП выглядят полностью здоровыми и не имеют никаких признаков болезни. Они нормально растут и набирают вес. Но большой дефект межпредсердной перегородки у детей может привести к появлению следующих симптомов:
- плохой аппетит;
- плохой рост;
- усталость;
- одышка;
- проблемы с легкими – например, пневмония.

Дефекты средних размеров могут не вызывать никаких симптомов, пока пациент не вырастет и не достигнет среднего возраста. Затем могут появиться следующие признаки:
- одышка, особенно во время физической нагрузки;
- частые инфекционные заболевания верхних дыхательных путей и легких;
- ощущение сердцебиения.
Если дефект МПП не лечить, в дальнейшем у пациента могут появиться серьезные проблемы со здоровьем, включая нарушения сердечного ритма и ухудшение сократительной функции сердца. По мере взросления детей с этим заболеванием у них может повышаться риск развития инсульта, так как тромбы, которые образуются в венах большого круга кровообращения, могут проходить через отверстие в перегородке из правого предсердия в левое и попадать в мозг.
Также со временем у взрослых пациентов с нелеченым большим дефектом в МПП может развиться легочная гипертензия и синдром Эйзенменгера, проявляющиеся:
- Одышкой, которая сперва наблюдается при физической нагрузке, а со временем и в состоянии покоя.
- Усталостью.
- Головокружениями и обмороками.
- Болью или ощущением сдавливания в грудной клетке.
- Отеками на ногах, асцитом (накопление жидкости в брюшной полости).
- Синеватым цветом губ и кожи (цианоз).
У большинства детей с дефектом МПП болезнь обнаруживают и лечат задолго до того, как возникают симптомы. Из-за осложнений, возникающих во взрослом возрасте, детские кардиологи часто рекомендуют закрывать это отверстие в раннем детстве.
Диагностика
Дефект в межпредсердной перегородке может быть обнаружен во время внутриутробного развития или после рождения, а иногда и в зрелом возрасте.
Во время беременности проводятся специальные скрининговые обследования, целью которых является раннее обнаружение различных пороков развития и заболеваний. Наличие дефекта в МПП можно выявить с помощью ультразвукового исследования, создающего изображение плода.
 Ультразвуковое исследование сердца плода
Ультразвуковое исследование сердца плода
После рождения ребенка обычно педиатр при осмотре обнаруживает сердечный шум, вызванный током крови через отверстие в МПП. Наличие этого заболевания не всегда удается выявить в раннем возрасте, как другие врожденные пороки сердца (например, дефект в перегородке, разделяющей правый и левый желудочек). Вызванный патологией шум – тихий, его услышать труднее, чем другие виды сердечных шумов, из-за чего это заболевание может быть выявлено в подростковом возрасте, а иногда и позже.
Если врач слышит и подозревает наличие врожденного порока, ребенка направляют к детскому кардиологу – врачу, который специализируется на диагностике и лечении детских сердечных заболеваний. При подозрении на дефект в межпредсердной перегородке он может назначить дополнительные методы обследования, включая:
- Эхокардиографию – обследование, состоящее в получении изображения структур сердца в режиме реального времени с помощью ультразвука. Эхокардиография может показать направление кровотока через отверстие в МПП и измерить его диаметр, а также оценить, сколько крови через него проходит.
- Рентгенографию органов грудной полости – это диагностический метод, использующий рентгеновские лучи для получения изображения сердца. Если у ребенка есть дефект в МПП, сердце может быть увеличено в размерах, так как правые отделы сердца вынуждены справляться с увеличенным количеством крови. Вследствие легочной гипертензии развиваются изменения в легких, которые можно обнаружить с помощью рентгенографии.
- Электрокардиография (ЭКГ) – запись электрической активности сердца, с помощью которой можно обнаружить нарушения сердечного ритма и признаки увеличенной нагрузки на его правые отделы.
- Катетеризация сердца – это инвазивный метод обследования, дающий очень детальную информацию о внутреннем строении сердца. Через кровеносный сосуд в паху или на предплечье заводится тонкий и гибкий катетер, который осторожно направляется внутрь сердца. Во всех сердечных камерах, аорте и легочной артерии измеряется давление. Для получения четкого изображения структур внутри сердца внутрь него вводится контрастное вещество. Хотя иногда достаточное количество диагностической информации можно получить с помощью эхокардиографии, во время катетеризации сердца можно закрыть дефект МПП с помощью специального устройства.
 Методы диагностики дефекта межпредсердной перегородки
Методы диагностики дефекта межпредсердной перегородки
Методы лечения
После выявления дефекта МПП выбор метода лечения зависит от возраста ребенка, размеров и расположения отверстия, тяжести клинической картины. У детей с очень маленьким отверстием оно может закрыться самостоятельно. Более крупные дефекты сами обычно не закрываются, поэтому их нужно лечить. Большинство из них можно устранить малоинвазивным путем, хотя при некоторых ДМПП необходимо проведение открытой операции на сердце.
Ребенку с небольшим отверстием в МПП, которое не вызывает никаких симптомов, может понадобиться только регулярно посещать детского кардиолога, чтобы убедиться в том, что не появилось никаких проблем. Часто эти маленькие дефекты закрываются сами по себе, без проведения какого-либо лечения, в течение первого года жизни. Обычно у детей с маленькими дефектами в МПП нет никаких ограничений в физической активности.
Если в течение года отверстие в МПП не закрылось само, врачам часто приходится устранять его до достижения ребенком школьного возраста. Это проводится тогда, когда дефект имеет крупные размеры, сердце увеличено в размерах или появились симптомы болезни.
Малоинвазивное эндоваскулярное лечение
До начала 1990-х годов открытые операции на сердце были единственным методом закрытия всех дефектов МПП. Сегодня, благодаря достижениям медицинских технологий, врачи для закрытия некоторых отверстий в МПП используют эндоваскулярные процедуры.
Во время такой малоинвазивной операции врач вводит тонкий и гибкий катетер в вену в паху и направляет его в сердце. Этот катетер содержит подобное зонту устройство в сложенном состоянии, которое называют окклюдером. Когда катетер достигает МПП, окклюдер выталкивают из катетера и закрывают им отверстие между предсердиями. Устройство закрепляют на месте, а катетер извлекают из тела. В течение 6 месяцев над окклюдером растет нормальная ткань.

Для точного направления катетера к отверстию врачи используют эхокардиографию или ангиографию.
Эндоваскулярное закрытие дефекта МПП намного легче переносится пациентами, чем открытые операции на сердце, поскольку для их проведения необходима лишь пункция кожи в месте введения катетера. Благодаря этому облегчается восстановления после вмешательства.
Прогноз после такого лечения прекрасен, оно успешно у 90% пациентов.
Открытые операции на сердце
Иногда дефект в МПП невозможно закрыть эндоваскулярным методом, в таких случаях проводят открытые операции на сердце.
Во время хирургического вмешательства кардиохирург делает большой разрез в грудной клетке, достигает сердца и ушивает отверстие. Во время операции пациент находится в условиях искусственного кровообращения.
Прогноз при открытых операциях на сердце по закрытию дефекта МПП прекрасен, осложнения развиваются очень редко. Пациент проводит в лечебном учреждении несколько дней, затем выписывается домой.
Послеоперационный период
После закрытия дефекта в МПП пациенты наблюдаются кардиологом. Медикаментозная терапия им нужна редко. Врач может проводить наблюдение с помощью эхокардиографии и ЭКГ.
После открытой операции на сердце основное внимание уделяется заживлению разреза грудной клетки. Чем моложе пациент, тем быстрее и легче проходит процесс восстановления. Если у больного появились одышка, повышенная температура тела, покраснение около послеоперационной раны или выделения из нее, следует немедленно обратиться за медицинской помощью.
Пациентам, которым проводилось эндоваскулярное лечение ДМПП, нельзя посещать спортзал или выполнять какие-то физические упражнения в течение недели. Спустя это время они могут вернуться к своему обычному уровню активности, проконсультировавшись перед этим с врачом.
Обычно дети после операции восстанавливаются очень быстро. Но и у них могут возникать осложнения. Немедленно обратиться за медицинской помощью следует в случае появления следующих симптомов:
- Одышка.
- Синий цвет кожи на губах.
- Ухудшение аппетита.
- Отсутствие увеличения веса или его снижение.
- Сниженный уровень активности у ребенка.
- Длительное повышение температуры тела.
- Выделения из послеоперационной раны.
Прогноз
У новорожденных небольшой дефект межпредсердной перегородки часто не вызывает никаких проблем, иногда закрывается без какого-либо лечения. Большие отверстия в МПП часто требуют эндоваскулярного или хирургического лечения.
Важными факторами, влияющими на прогноз, являются размер и расположение дефекта, величина кровотока через него, наличие симптомов болезни.
При своевременном проведении эндоваскулярного или хирургического закрытия дефекта прогноз прекрасный. Если этого не сделать, у людей с большим отверстием в МПП повышается риск развития:
- нарушений сердечного ритма;
- сердечной недостаточности;
- легочной гипертензии;
- ишемического инсульта.
У детей с врожденными пороками сердца примерно в 6-10% случаев встречаются единичные или множественные отверстия на перегородке, которая находится между двумя предсердиями сердца. Это заболевание называется «дефект межпредсердной перегородки», и оно приводит к патологическому сбросу крови влево, постепенному развитию нарушений гемодинамики и развитию сердечной недостаточности и легочной гипертензии.
Особенности заболевания
Предсердная перегородка формируется у плода во время его внутриутробного развития. Она закладывается из двух гребней, один из которых растет вверх от атриовентрикулярного соединения (первичная часть перегородки — ее нижняя треть), второй — от основания сердца вниз. Примерно в середине перегородки находится овальная ямка, которая у плода не закрыта и представляет собой окно — естественный компонент кровообращения во время внутриутробного развития ребенка. У новорожденных закрытие овального окна происходит в первые недели после появления на свет. Если же закрытия не произошло, ставится диагноз «дефект предсердной перегородки».
До 10% среди всех ВПС принадлежит именно дефектам межпредсердной перегородки (ДМПП), причем этот порок является самостоятельным (изолированным). Что касается сочетанных, сложных ВПС, то в таких случаях ДМПП соседствует с другими нарушениями строения сердца уже у 30-35% детей с пороками. В большинстве случаев он ассоциируется с такими ВПС и другими врожденными заболеваниями сердечно-сосудистой системы:
- стеноз легочной артерии;
- недостаточность митрального или трикуспидального клапана;
- аномалии развития легочных вен;
- коарктация аорты;
- открытый артериальный проток;
- дефект межжелудочковой перегородки;
Незакрывшиеся отверстия в предсердной перегородке могут представлять собой и варианты недоразвития одной из ее частей. В любом случае, один или множественные дефекты обуславливают нарушения гемодинамики внутри сердца. Давление крови в левом предсердии выше давления в правом предсердии на 8-10 мм.рт.ст. При наличии дефекта оно может выравниваться, либо приближаться к равному. Происходит заброс крови через шунт слева направо, что провоцирует увеличение легочного кровотока и перегрузку правого желудочка, при этом выраженность патологических изменений напрямую зависит от размера дефекта в предсердной перегородке и податливости желудочков.
Так как в первое время жизни толщина стенок желудочков одинакова, то в период диастолы они растягиваются равномерно, патологический сброс небольшой. С возрастом растет и уменьшение сосудистого сопротивления, а через шунт сбрасывается все более значительное количество крови.
Правые отделы сердца из-за хронической перегрузки увеличиваются в размерах, но даже на данном этапе симптомов патологии может не быть. Только появление признаков легочной гипертензии (обычно к 2-3 годам и старше), а также сердечной недостаточности вызывает развитие симптоматики (чем крупнее дефект, тем раньше наблюдаются патологические признаки у ребенка).
Многие ДМПП спонтанно закрываются в первые годы жизни (речь идет о дефектах небольшого размера — до 2-5 мм.). Кроме подразделения по размеру, отверстия в межпредсердной перегородке классифицируются следующим образом:
- Первичный дефект, расположенный в нижней трети перегородки. Такие отверстия локализованы вблизи атриовентрикулярных клапанов, которые деформированы, либо наблюдается их дисфункция. Первичные дефекты представляют собой аномалии развития эндокардиальных подушечек. Изредка у взрослых возникает синдром Лютембаше — комбинация ДМПП с приобретенным стенозом митрального клапана , который возникает на фоне перенесенного ревматизма.
- Вторичный дефект, находящийся в верхней части перегородки или зоне овальной ямки (до 80% от всех ДМПП). Такие дефекты не следует путать с заболеванием «незаращение овального отверстия», которое, при малых размерах, вообще не влияет на продолжительность жизни и гемодинамику. Вторичные дефекты чаще всего сочетаются и с другими пороками сердца, с аневризмами. К группе вторичных ДМПП также относится редкий дефект венозного синуса.
Причины дефекта межпредсердной перегородки
Образование ДМПП связано с различными нарушениями в развитии плода в эмбриональном периоде. Эти нарушения касаются недоразвития частей межпредсердной перегородки и эндокардиальных валиков. Несмотря на то, что многие случаи дефектов являются спорадическими, есть множественные данные наследственной передаче патологии в тех семьях, где мать, отец или ближайшие родственники уже имели ВПС. Нередко ДМПП как семейные случаи появляются в комбинации с атриовентрикулярной блокадой, либо с недоразвитием костей кистей (синдром Холта-Орама).
Влияние тератогенных факторов на плод также может привести к развитию патологии. К ним относятся:
- инфекции у беременной женщины, перенесенные ею в первом триместре беременности — краснуха, ветрянка, цитомегаловирус, грипп, герпес, сифилис и многие другие;
- острые лихорадочные состояния;
- наличие нескорректированных эндокринопатий, особенно, сахарного диабета;
- прием лекарств, обладающих токсическим действием на плод;
- рентгеновское обследование матери, попадание под воздействие ионизирующей радиации;
- ранний токсикоз вплоть до угрозы выкидыша;
- работа матери на вредном производстве;
- прием алкоголя, наркотиков;
- неблагоприятная экология в месте проживания.
Привести к появлению множественных пороков сердца, а также аномалий развития этого органа вкупе с другими нарушениями в организме могут хромосомные мутации, случающиеся при зачатии. Так, дефект предсердной перегородки может становиться частью тяжелых генетических заболеваний — синдрома Гольденхара, синдрома Вильямса, синдрома Эллиса-Ван Кревельда и многих других.
Симптоматика болезни

Данный порок сердца имеется у ребенка с самого рождения. Тем не менее, его симптомы появляются намного позже — через несколько недель, месяцев, либо даже лет. При прослушивании сердца в родильном доме, как правило, отклонений не обнаруживается. Только позже появляется характерный шум в сердце, который, впрочем, может быть и очень слабым или не слышен вообще. Отсутствие симптоматики нередко приводит к позднему распознаванию порока, когда у ребенка уже имеются серьезные осложнения.
Чем больше размер отверстия в предсердной перегородке и меньше величина сопротивления легочной артерии, тем быстрее появляется клиническая картина ДМПП. Обычно ребенок до определенного возраста растет и развивается наравне со сверстниками, но затем становятся заметны первые признаки — более скорая утомляемость и непереносимость высоких физических нагрузок. Но когда данной порок сердца сочетается с другими ВПС, а нарушения гемодинамики более значимы, симптоматика может быть и ранней, и более явной. В целом, возможны следующие составляющие клиники заболевания:
- тахикардия;
- чувство сердцебиения;
- одышка при напряжении;
- формирование «сердечного горба»;
- усиление пульсации правого желудочка и легочной артерии;
- шумы в сердце;
- цианоз (как правило, выражен слабо);
- стойкая бледность кожи;
- холодность конечностей;
- слабость;
- головокружения, склонность к обморокам;
- увеличение размеров печени.
У 5% детей с вторичным пороком предсердной перегородки уже к году возникает тяжелая сердечная недостаточность, что, как правило, связано с наличием крупного дефекта венозного синуса. У таких больных всегда имеется отставание в физическом развитии, а порой и — сопутствующие пороки и аномалии других органов из-за существования генетических синдромов. При отсутствии операции на сердце большинство из этих больных умирает в раннем возрасте. Возможен еще один неблагоприятный исход заболевания, когда оно протекает бессимптомно многие годы и проявляется эмболическим инсультом у больного, что нередко случается во время беременности у женщин с ВПС.
Возможные осложнения
Как правило, без устранения дефекта на фоне гиперволемии малого круга кровообращения часто возникают респираторные заболевания — бронхиты, пневмонии, которые длительно не поддаются лечению, сопровождаются сильным кашлем с влажными хрипами и одышкой. Изредка может наблюдаться кровохаркание. Как правило, к 20-ти годам у больного начинают появляться осложнения:
- легочная гипертензия — перегрузка правой части сердца, возникновения застоя в легочном круге и повышения в нем давления;
- сердечная недостаточность — нарушение работы сердца в части его насосной функции, в результате чего орган не справляется с обеспечением тканей кислородом;
- аритмии — изменения сердечного ритма вплоть до тех, что угрожают внезапной остановкой сердца ;
- синдром Эйзенменгера — необратимые изменения в легких на фоне легочной гипертензии;
- парадоксальная эмболизация — проход тромбов из вен через имеющийся в предсердной перегородке дефект;
- тромбоэмболия — формирование и отделение тромбов от стенок сосудов и закупорка ими жизненно важных артерий — легочной, церебральных. Подробнее о диагностике и признаках тромбоэмболии на экг
Предотвратить эти последствия и следующую за ними инвалидность и смерть способно только лишь своевременное хирургическое вмешательство.
Проведение диагностики
Способы диагностики заболевания у детей и взрослых следующие:
- ЭКГ. Имеются признаки увеличения правого предсердия и правого желудочка, их перегрузка, если у больного уже возникает легочная гипертензия. Может выявиться резкое отклонение электрической оси влево из-за смещения уменьшенной ветви левой ножки пучка Гиса . При осложнениях на кардиограмме встречаются признаки атриовентрикулярной блокады , слабости синусового узла. При дефекте венозного синуса появляется нижнепредсердный ритм.
- Рентгенография грудной клетки. Есть усиление легочного рисунка, расширенность корней легких, выбухание правого предсердия, более выраженная пульсация легочных корней.
- УЗИ сердца с допплерографией (у взрослых — чреспищеводная ЭхоКГ). Обнаруживаются гипертрофия, дилатация левых отделов, при легочной гипертензии — также и правых отделов сердца. Может быть визуально заметен собственно дефект межпредсердной перегородки (на данном этапе его дифференцируют с открытым овальным окном). Проводится анализ наличия сопутствующих пороков и аномалий, оценивается степень сброса крови.
- Катетеризация сердца (зондирование его полостей). Показана перед операцией по поводу устранения порока сердца, а также при подозрении на легочную гипертензию при противоречивых данных других обследований. При катетеризации выполняют пробу с ингаляцией кислорода и пробу с аминофиллином, которые позволят оценить степень обратимости легочной гипертензии.
- Ангиография, МРТ-ангиография. Как правило, эти методы требуются для выявления аномального дренажа вен легких и дисфункции желудочков как сопутствующих ДМПП патологий.
ДМПП следует дифференцировать с дефектом межжелудочковой перегородки, триадой Фалло, аномальным дренажем легочных вен, открытым артериальным протоком и другими пороками сердца, а также их комбинацией. Вторичные дефекты предсердной перегородки следует также отличать от функционального систолического шума в сердце, незаращения овального отверстия.
Когда нужно срочно обратиться к врачу
В том случае, если ДМПП не был диагностирован в раннем возрасте, родители могут вообще не подозревать о его существовании. Нередко врачи рекомендуют повременить с операцией до определенного возраста малыша (как правило, вмешательства делают после 3-4 лет), и он продолжает жить и расти с имеющимся дефектом в предсердной перегородке. В любом случае, нужно срочно обратиться к врачу при появлении следующих симптомов у ребенка:
- посинение кожи;
- резкое усиление утомляемости, слабость;
- одышка;
- отеки руки и ног;
- аномальное сердцебиение;
- нарушения пульса;
- боли в области сердца.
Эти признаки отражают развитие той или иной степени сердечной недостаточности , в связи с чем операцию, возможно, придется выполнять раньше намеченного срока.
Методы лечения
Дефекты менее 3 мм. в диаметре часто закрываются самостоятельно. Обычно это происходит к 1,5 годам возраста ребенка. Что касается первичных дефектов, а также дефектов венозного синуса, они никогда не закрываются самопроизвольно. Обычно без операции к 20-30 годам возникает легочная гипертензия и сердечная недостаточность, но это может происходить и намного раньше. Поэтому операция показана всем больным с ДМПП, но не раньше, чем в 3-5 лет. Показания к более скорому выполнению вмешательства следующие:
- гиперплазия отделов сердца;
- рецидивирующие пневмонии;
- увеличение стенок легочной артерии;
- серьезная задержка физического развития;
- прогрессирование сердечной недостаточности;
- наличие сопутствующих пороков сердца.
До операции детям показано регулярное наблюдение у кардиолога и выполнение курсов медикаментозного лечения:
- диуретики при отеках, симптомах нарушения легочного кровообращения;
- бета-блокаторы для снижения давления, устранения нарушений ритма сердца;
- тромболитики для понижения свертываемости крови для недопущения угрозы тромбообразования;
- сердечные гликозиды для расширения сосудов и увеличения объема выталкиваемой сердцем крови.
Существует несколько видов операций, которые в настоящее время применяются при ДМПП. Выбор конкретной методики зависит от размера дефекта и его типа. Есть два основных вида операций и множество их разновидностей:
- пластика (заплатка из перикарда или синтетической ткани) или ушивание дефекта при создании условий искусственного кровообращения;
- окклюзия дефекта устройством Амплатцера и другими устройствами (обычно используется при малых размерах отверстия и его правильной форме).
Обычно при раннем выполнении операции в детском возрасте осложнения встречаются не более, чем в 1-4% случаев (тромбозы, перфорация стенки сосуда, АВ-блокада и т.д.), летальность не превышает 0,1%. Как правило, дилатация камер сердца подвергается обратному развитию после устранения дефекта. Во взрослом возрасте даже после операции могут сохраняться имеющиеся осложнения — легочная гипертензия, аритмии.
Образ жизни при данной патологии

После операции и до ее выполнения ребенку нельзя заниматься профессиональным спортом, строго запрещены физические перегрузки, тяжелый труд. В первые недели от проведения вмешательства следует носить специальный бандаж, который не даст швам разойтись, соблюдать постельный режим, а затем нужно начинать понемногу двигаться, глубже дышать. Нельзя принимать душ и ванну, пока швы полностью на заросли, а только аккуратно протирать тело влажной губкой.
При пороках сердца следует обязательно придерживаться здорового образа жизни, правильно питаться. Нужно по возможности не допускать респираторных патологий в первый год после вмешательства, а также до его выполнения. Умеренные физические нагрузки показаны всем прооперированным пациентам — гимнастика, прогулки, плавание и т.д. У кардиолога после операции желательно наблюдаться раз в год до конца жизни. Нельзя забывать принимать все лечебные и профилактические средства, которые назначил врач.
Беременность и роды
Малые размеры ДМПП у женщины обычно позволяют ей выносить и родить ребенка без проблем. Но при уже имеющихся осложнениях в виде легочной гипертензии , сердечной недостаточности, аритмии, при крупных размерах дефекта может возникнуть опасное для жизни матери и плода состояние при гестации, ведь нагрузка на сердце в этот период серьезно возрастает. Именно поэтому кардиологи настоятельно рекомендуют проводить хирургическое лечение в детском или подростковом возрасте, либо планировать беременность после прохождения курса консервативной терапии. В любом случае, следует наблюдаться у специалиста, а также на раннем сроке выполнять УЗИ сердца плода для обнаружения несовместимых с жизнью или сочетанных пороков, которые могут быть обусловлены отягощенной наследственностью.
Прогноз патологии
Прогностический расчет основывается на сроках проведения операции и наличии возникших до ее выполнения осложнений. Без операции в раннем детском возрасте течение болезни в 95% случаев доброкачественное. Тяжелые нарушения кровообращения и смерть в первый год жизни наблюдаются редко. Без лечения средняя длительность жизни — 40 лет, 15% больных погибает до 30 лет. Около 7% доживает до 70 лет, но уже к возрасту 45-50 лет становится инвалидами.
При устранении дефекта в детстве риск осложнений мал, больные, как правило, проживают полноценную жизнь.
В некоторых случаях все-таки возможно развитие различных видов аритмии в возрасте 45-60 лет. При оперативном закрытии дефекта после 20-25 лет высок риск сокращения продолжительности жизни из-за наличия необратимой легочной гипертензии и сердечной недостаточности.



